Rasayanik Padarth रासायनिक पदार्थ क्या है रासायनिक पदार्थ किसे कहते हैं रासायनिक पदार्थ में कौन-कौन सी धातु आती है इन सभी के बारे में आज हम चर्चा करने वाले हैं रासायनिक पदार्थ रासायनिक पदार्थ व पदार्थ होते हैं जिनकी संरचना और विशिष्ट गुना वाला पदार्थ का एक अनूठा रूप होता है रासायनिक पदार्थ रासायनिक यौगिक किया एक तत्व का रूप ले सकते हैंयदि दो या दो से अधिक रासायनिक पदार्थों को बिना प्रतिक्रिया किए जोड़ा जा सकता है तो वह एक रासायनिक मिश्रण बना सकते हैं आज इस आर्टिकल के माध्यम सेहम रासायनिक पदार्थों के बारे में चर्चा करेंगे जो भी विद्यार्थी कॉम्पिटेटिव एक्जाम के लिए तैयारी कर रहा है उनके लिए आज का यह लेख बहुत ही उपयोगी होने वाला है तो आप हमारे साथ बने रहे.
कार्बन
कार्बन भू
प्रॉपर्टी में पाया जाने वाला 17 व अति बाहुल्य तत्व है यह प्रकृति में स्वतंत्र एवं संयुक्त अवस्था में बहुत आयात से पाया जाता है तत्व अवस्था से यह कोयला ग्रेफाइट तथा हीरा में मिलता है जबकि संयुक्त अवस्था में यह धातु कार्बोनेट हाइड्रोकार्बन तथा वायु में कार्बन डाइऑक्साइड गैस के रूप में मिलता है यह कहा जा सकता है कि कार्बन संसार का सबसे चंचल तत्व है जो अन्य तत्व जैसेडाई हाइड्रोजन दी ऑक्सीजन क्लोरीन सल्फर आदि से योग करके जीवित उत्तकों से दावों एवं प्लास्टिक तक का निर्माण करता हैकार्बन का एक रेडियोएक्टिव समस्थानिक है जिसकोअर्ध आयु 5800 वर्ष लगभग है इसका उपयोग जीवाश्म की आयु निर्धारण में होता है
कार्बन की विशेषताएं निम्न प्रकार है
कार्बन परमाणु का संकेत C है जिसकी परमाणु संख्या 6 तथा द्रव्यमान संख्या 12 होती है
कार्बन संयोग होता है इसमें संयुक्त इलेक्ट्रॉनों की संख्या चार है कार्बन की ज्यामिति चतुष्कलकीय होती है
हाइड्रोजन की अतिरिक्त कार्बन अपनी संयोजकता पूर्ण करने के लिए कार्बन परमाणु से ही सहयोग का नए पदार्थ बनाने की क्षमता रखता
अपररूपता
जब कोई तत्व दो या दो से अधिक रूपों में पाया जाता है जिसके भौतिक तथा कुछ रासायनिक को अलग-अलग हो अपरूप कहलाते हैं इस गुण को अपररुपता कहते हैं
कार्बन के अपररूप
क्रिस्टलीय अक्रिस्टलीय
क्रिस्टलीय
हीरा ग्रेफाइट फुलरीन
अक्रिस्टलीय
- कोल – काजल
- कोक – गैस कार्बन
- कास्ट – चारकोल
कार्बन के अपररूप
- क्रिस्टलीय 2. अक्रिस्टलीय
क्रिस्टलीय अपररूप – जिन पर रूपों में कार्बन परमाणु निश्चित ज्यामितिय संरचना में पाए जाते हैं यह क्रिस्टलीय अपररूप कहलाते हैं जैसे हीरा ग्रेफाइट फुलरीन
हीरा
हीरा में क्रिस्टलीय जालक होता है हीरे में एक कार्बन चार अन्य कार्बन परमाणुओं से चतुष्कल्प किए ज्यामिति में जुड़कर त्रिविमीय जलक का निर्माण करता है इस प्रकार विस्तृत सहसंयोजक बंधन को तोड़ना कठिन कार्य होता है अतः हीरा पृथ्वी पर पाया जाने वाला सर्वाधिक कठोर पदार्थ है
यह विद्युत तथा ताप का कुचालक होता है
यह प्राकृतिक स्रोत किंबरलाइट का पत्थर है
हीरा किसी भी विलियन में नहीं घुलता है
संसार में मुख्यतः कुलीनान (3032केरेट) कोहिनूर (186 कैरेट), पिट (136.02 केरेट), तथा हॉप (445 कैरेट) प्रमुख हीरे हैं
कुछ हीरे काले रंग के होते हैं जिन्हें बोट के नाम से जाना जाता है तथा यह कांच को आसानी से काट देता है
हीरा पूर्ण आंतरिक परावर्तन के कारण बहुत चमकता है
हीरे का उपयोग
हीरा जवाहर तो में नगीनों के रूप में
कांच को काटने में
चट्टानों या पत्थर काटने की शो मशीन में
धार तेज करने के लिए अपघर्षक के रूप में
विद्युत प्रकाश लैंप में टंगस्टन तंतु बनाने में
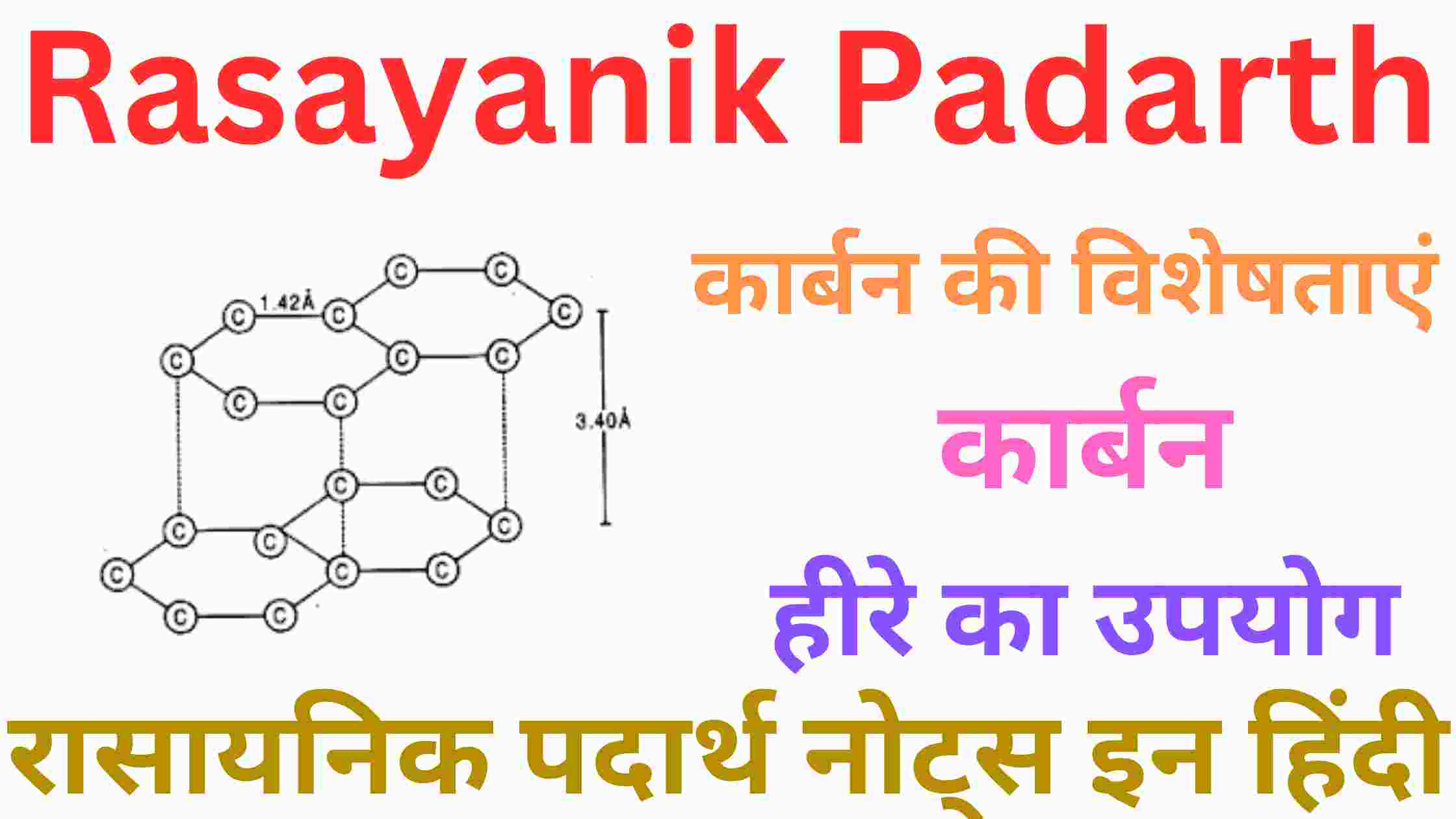
ग्रेफाइट
यह गहरी धूसर रंग का चमकीला पदार्थ है ग्रेफाइट प्रत्यय संरचना के रूप में होता है यह पढ़ने परस्पर वंडरवॉल बल द्वारा जुड़ी रहती है प्रत्येक परत में कार्बन परमाणु तीन अन्य कार्बन परमाणुओं से तीन सिग्मा बंध द्वारा शतकोणीय वाले के रूप में व्यवस्थित होते हैं इनमें प्रत्येक कार्बन के पास एक मुक्त इलेक्ट्रॉन होता है यह मुक्त इलेक्ट्रॉन गतिशील होता है इसलिए ग्रेफाइट विद्युत का सुचालक होता है ग्रेफाइट को परते आसानी से एक दूसरे पैर फिसल सकती है यही कारण है कि ग्रेफाइट मुलायम तथा चिकना होता है
उपयोग
- पेंसिल बनाने में
- इलेक्ट्रोड बनाने में
- लोहे पर पॉलिश करने में लिया जाता है
- नाभि के भट्टे में मंदक के रूप में
- उच्च ताप पर जिन मशीनों में तेल का प्रयोग स्नेह के रूप में नहीं हो सकता है उनमें ग्रेफाइट शुष्क स्नेहक का कार्य करता है
हीरा और ग्रेफाइट में अंतर
| हीरा | ग्रेफाइट |
| यह कठोर होता है | यह मुलायम होता है |
| यह विद्युत का कुचालक होता है | यह विद्युत का सुचालक होता है |
| यह पारदर्शी व रंगहीन होता है | यह अपारदर्शी व रंगीन होता है |
| इससे कांच को काटा जा सकता है | इससे पेंसिल व रंग बनाए जाते हैं |
| इसकी संरचना चतुश्फल की होती हैं | इसकी संरचना सेट कोनिया जलक होती है |
फूलरीन
यह कार्बन का तीसरा क्रिस्टलीय अपरूप है हीलियम अंग आदि अक्रिय गैसों की उपस्थिति में जब ग्रेफाइट को विद्युत पार्क में गर्म किया जाता है तब फुल रेन का निर्माण होता है फुलरेन की संरचना फुटबॉल आकृति में पिंजरानुमा होती है
फुलरीन के एक अणु में 60 से 70 कार्बन परमाणु होते हैं सर्वाधिक स्थाई फुलरीन है जिसे बकमिंस्टर भी कहते हैं गोलाकार फुलरीन को बाकी बोल भी कहते हैं
यह भी पढ़े – Elements Compounds And Mixtures Part 3 | तत्व यौगिक एवं मिश्रण नोट्स इन हिंदी पार्ट 3
उपयोग
- उच्च ताप पर अतिचालक होने के कारण तकनीकी दृष्टि से महत्वपूर्ण होते हैं
- आणविक बेरिंग में
- अक्रिस्टलीय अपरूप इनकी निश्चित संरचना नहीं होती है
इसके उदाहरण निम्न है
कास्ट कोयला लकड़ी को जलाने पर कार्बन का अक्रिस्टलीय अपरूप कोयले के रूप में प्राप्त होता है इसका उपयोग ईंधन के रूप में होता है
कोक
के कोयले के पंजन आसवन से कोक प्राप्त होता है जिसका उपयोग भटियो में ईंधन के रूप में होता है
चारकोल
लकड़ी तथा कार्बनिक यौगिक को वायु की अनुपस्थिति में गर्म करने पर चारकोल प्राप्त होता है इसका उपयोग द्रवो की अशुद्धियों को दूर करने में किया जाता है
काजल कार्बनिक पदार्थ को उच्च ताप पर जलने से मुक्त हुआ कार्बन काजल कहलाता है
इसका उपयोग सौंदर्य प्रसाधनों में स्याही बनाने में फोटोकॉपिर मशीन तथा जूते की पॉलिश में किया जाता है
कोयला
यह ऊर्जा का अनवीनीकरण स्रोत है यह एक ठोस कार्बनिक पदार्थ होता है जिसके प्रयोग ईंधन के रूप में करते हैं विभिन्न प्रकार के कोयले में कार्बन की मात्रा भी अलग-अलग होती है
हाइड्रोकार्बन
कार्बन तथा हाइड्रोजन से बने योगी को हाइड्रोकार्बन कहते हैं
हाइड्रोकार्बन का प्रमुख प्राकृतिक स्रोत पेट्रोलियम है
संपूर्ण विश्व में योगी को एक ही नाम से जाना जाए इसके लिए वर्तमान में एक नवीन पद्धति प्रचलित थी जिसे अंतरराष्ट्रीय विशुद्ध और अनुपयुक्त रसायन संग पद्धति कहा जाता है
हाइड्रोकार्बन के नामकरण में योगी के अणु में उपस्थित कार्बन परमाणु की संख्या के आधार पर उसका पूर्ण लगन लिखा जाता है
अनु में उपस्थित बंद के आधार पर उसका अनु लगन लिखा जाता है
पूर्व लग्न तथा अनु लगन को जोड़कर हाइड्रोकार्बन का पूरा नाम लिखा जाता है
हाइड्रोकार्बन को दो वर्गों में विभाजित किया जा सकता है
- एलिफेटिक अचक्रीय हाइड्रोकार्बन
- एरोमेटिक चक्रीय हाइड्रोकार्बन
यह भी पढ़े – Atoms And Molecules | परमाणु एवं अणु नोट्स इन हिंदी
Atoms And Molecules Part 2 | परमाणु एवं अणु नोट्स इन हिंदी पार्ट 2

Hello, में तानिया gurusmiles.org पोर्टल के माध्यम से शिक्षक व शिक्षार्थियों को शिक्षा विभाग की लेटेस्ट न्यूज़ प्रदान करने के लिए तत्पर हू आप इस पोर्टल के माध्यम से शिक्षा विभाग की समस्त खबरे प्राप्त कर सकते है इस पोर्टल के माध्यम से सैंपल पेपर || जॉब्स अलर्ट || रिजल्ट || उत्तर कुंजी || स्टडी नोट्स प्राप्त कर सकते है






